CONSTRUCCIÓN Y OPERACIÓN DE BATERÍA DE PLOMO-ÁCIDO
Envase
: El recipiente está hecho de caucho duro o plástico resistente a los ácidos. Está dividido en compartimentos.
Cada compartimento forma una celda de 2v. En la parte inferior del puente de contenedores se proporcionan espacios para la recolección de sedimentos. Esto evita el peligro de descarga eléctrica en el circuito.
: Hay dos tipos de placa de batería positiva y negativa. Cada placa está fabricada a partir de un marco o rígido de una aleación de plomo y antimonio. La función de la rejilla es retener material activo y transportar corriente. El material activo en la placa positiva es LED rojo (Pb3O4) y en la placa negativa es litargirio (PbO). El grupo de placas negativas contiene un
placa más que el grupo de placas positivas.
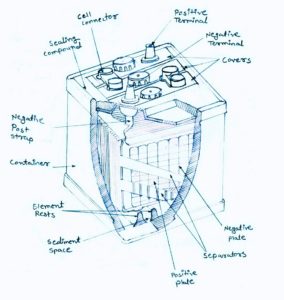 construcción y funcionamiento de la batería
construcción y funcionamiento de la batería Separador
: Para evitar el contacto directo y por tanto el cortocircuito entre las placas positiva y negativa, se inserta entre ellas una fina lámina de algún material no conductor, llamada separador.
Cobertura celular:
Electrólito
: Después del montaje completo, la batería se llena de electrolito. Es una solución de ácido sulfúrico (H2So4) que contiene aproximadamente una parte de ácido sulfúrico y dos partes de agua en volumen.
FUNCIONAMIENTO CON BATERÍA
La diferencia de potencial entre dos metales sumergidos en un electrolito se denomina voltaje de celda. Una batería convierte la energía química del metal sumergido en el electrolito en energía eléctrica mediante el proceso electroquímico de oxidación-reducción.
Descargando
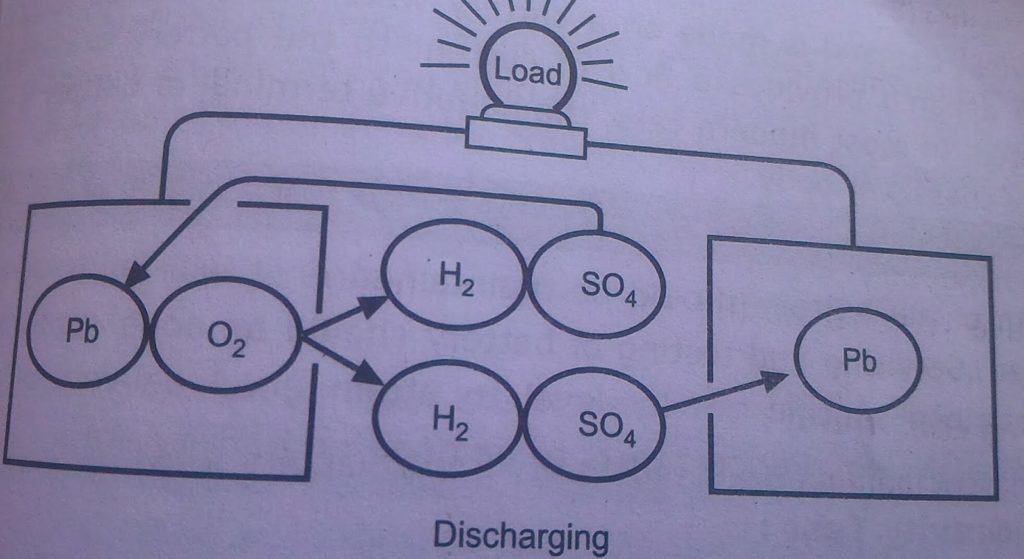 Descarga de reacción química de la batería
Descarga de reacción química de la batería Reacción química de carga y descarga de batería.
Reacción química de carga y descarga de batería.Se dice que esta es la condición de carga de la batería.
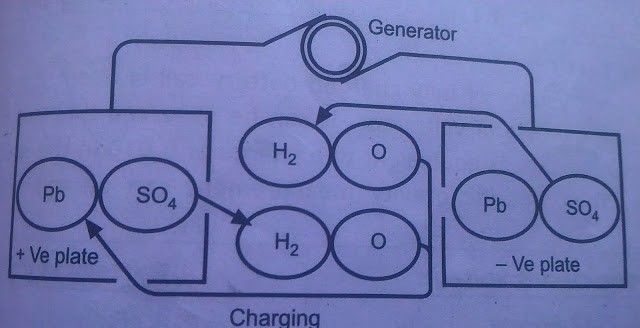 cómo cargar la batería
cómo cargar la bateríaDhatrak









