1. Estrutura e cristalização de metal puro
1. Estrutura cristalina do metal
Os metais são cristais no estado sólido.
A estrutura cristalina está relacionada às propriedades, deformação plástica e transformações de fase de tratamento térmico dos metais.
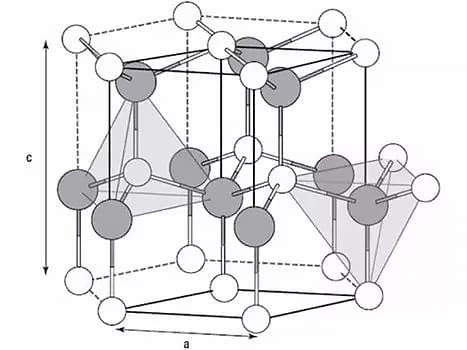
As três redes mais comuns em metais são a rede cúbica de corpo centrado, a rede cúbica de face centrada e a rede hexagonal compactada.
Os defeitos cristalinos podem ser classificados em três categorias com base em suas formas geométricas: defeitos pontuais, defeitos lineares e defeitos planos.
2. Cristalização de metais
O processo pelo qual um metal passa do estado líquido para o estado sólido (cristalino) é conhecido como cristalização do metal.
(1) Curva de resfriamento e fenômeno de super-resfriamento
A curva de resfriamento é um gráfico que mostra a relação entre temperatura e tempo durante o processo de resfriamento de um material. A curva de resfriamento de um cristal metálico pode ser determinada usando métodos de análise térmica. O processo envolve derreter o metal para atingir uma temperatura tão uniforme quanto possível, resfriá-lo a uma velocidade definida, registrar as mudanças de temperatura ao longo do tempo e traçar os dados em um gráfico temperatura-tempo para obter a curva de resfriamento, conforme mostrado na Figura 1. .
O calor latente de cristalização liberado durante a cristalização neutraliza a perda de calor do metal para o exterior, fazendo com que apareça uma linha horizontal na curva de resfriamento. A temperatura correspondente a esta linha é a temperatura real de cristalização do metal.
Experimentos mostram que a temperatura real de cristalização (T1) do metal é sempre inferior à temperatura teórica de cristalização (T0). Este fenômeno é conhecido como super-resfriamento. O super-resfriamento é um requisito para que a cristalização ocorra. A diferença entre T0 e T1, △T = T0 – T1, é conhecida como grau de super-resfriamento.
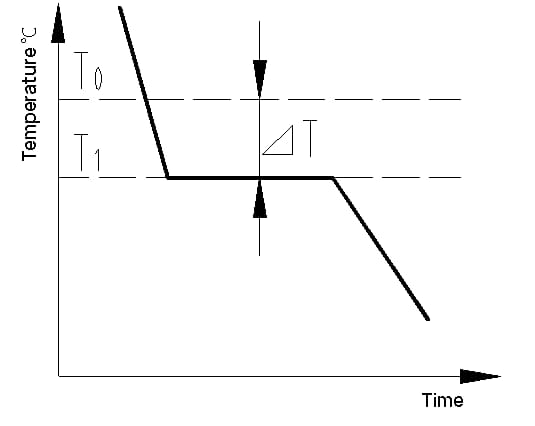
Fig. 1 curva de resfriamento de cristal de ferro puro
(2) Processo de Cristalização
O processo de cristalização envolve a criação e expansão de núcleos. Este processo é conhecido como nucleação e crescimento.
3. Transformação isomérica de metais
O fenômeno no qual um metal se transforma de uma estrutura reticulada para outra à medida que a temperatura muda no estado sólido é conhecido como transformação isomórfica.
Alguns metais que exibem essa transformação incluem ferro, cobalto, titânio, estanho e manganês.
Cristais do mesmo elemento metálico que existem em diferentes formas de rede são chamados de cristais alotrópicos do metal.
2. Estrutura e cristalização da liga
Fase: Refere-se aos componentes uniformes dentro de uma liga (ou metal puro) que possuem a mesma composição, estrutura e propriedades e são separados uns dos outros por uma interface.
1. Estrutura de fase da liga
A estrutura de fases nas ligas pode ser dividida em dois tipos com base na interação entre os elementos constituintes: solução sólida e composto metálico.
(1) Solução Sólida: Quando a liga líquida solidifica, os elementos ainda podem se dissolver uns nos outros para formar uma fase na qual os átomos de um elemento são dispersos por toda a rede de outro elemento. Esta fase é conhecida como solução sólida.
(2) Composto Metálico.
2. Diagrama de estado da liga binária
O diagrama de fases da liga, também conhecido como diagrama de equilíbrio da liga ou diagrama do estado da liga, é um diagrama que ilustra a relação entre a temperatura, a composição e o estado de uma liga sob condições de equilíbrio. Ele descreve as leis de mudança estrutural de ligas com composições variadas à medida que são resfriadas lentamente ou aquecidas até o infinito.
O diagrama de fases da liga é uma ferramenta importante para selecionar a composição correta da liga, analisar a microestrutura da liga, estudar suas propriedades e determinar os processos de fundição, forjamento e tratamento térmico.
(1) Diagrama de fases homogêneas: Este tipo de diagrama representa um sistema de liga onde dois componentes podem ser infinitamente miscíveis nos estados líquido e sólido. Durante a solidificação, a liga forma uma solução sólida a partir da fase líquida, processo conhecido como transformação homogênea.
(2) Diagrama de fases eutéticas: Neste diagrama, dois componentes são completamente miscíveis no estado líquido e apresentam uma transformação eutética. A Transformação Eutética refere-se à cristalização simultânea de duas fases sólidas com uma composição específica a partir de uma fase líquida uniforme com uma composição específica a uma temperatura específica.
(3) Diagrama de fases peritéticas: Neste diagrama, dois componentes são infinitamente miscíveis no estado líquido e formam uma solução sólida finita no estado sólido. Há também um estado de transformação peritética. A Transformação Peritética refere-se à reação entre a fase líquida de um determinado componente e a fase sólida de outro componente, que resulta na formação de uma nova fase sólida a temperatura constante.
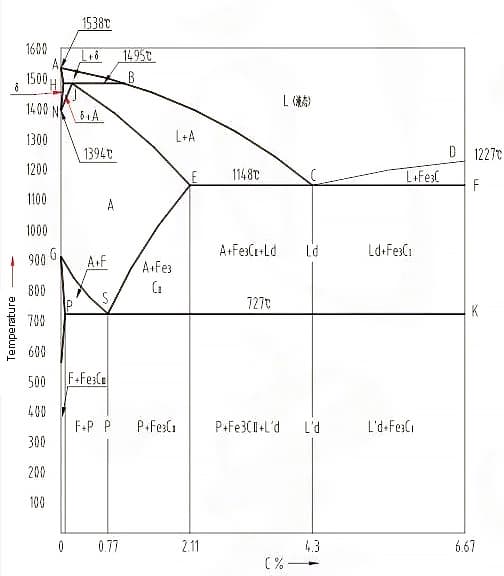
3. Diagrama de fases de ferro-carbono
1. Diagrama de fases de ferro-carbono
O aço é uma liga de ferro-carbono com uma faixa de composição específica.
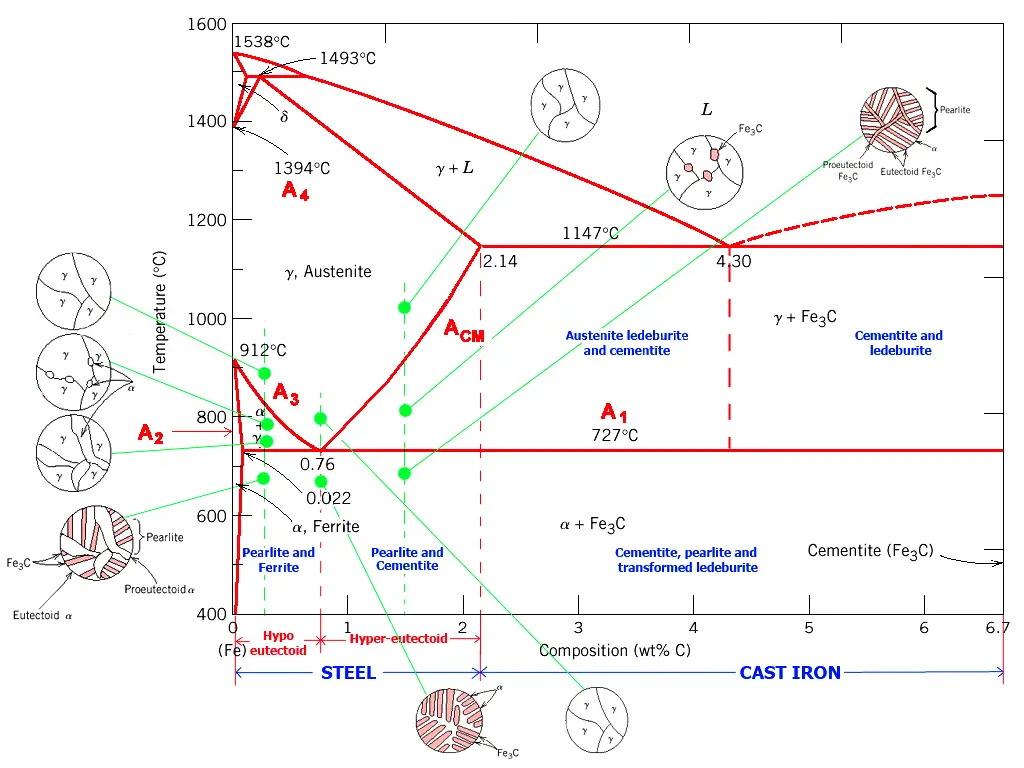
O diagrama de fases da liga ferro-carbono ilustra as várias estruturas de equilíbrio das ligas ferro-carbono com composições variadas em diferentes temperaturas, conforme representado no diagrama de fases Fe-Fe3C.
A partir do diagrama de fases Fe-Fe3C, podemos determinar a temperatura na qual ocorre a transformação de fase em uma liga ferro-carbono de determinada composição, também conhecida como ponto crítico.
Ao analisar o diagrama de fases Fe-Fe3C, é possível prever o processo de transformação de fase em diferentes regiões de temperatura e a estrutura potencial de equilíbrio após o resfriamento à temperatura ambiente.
Consulte os pontos característicos no diagrama de fases Fe-Fe3C para obter uma descrição de cada ponto no diagrama de fases da liga ferro-carbono e as linhas características para obter uma descrição de cada linha.
De acordo com o diagrama de fases da liga ferro-carbono, são diferenciados o aço carbono com teor de carbono inferior a 2,11% e o ferro fundido com teor de carbono superior a 2,11%.
Com base nas características estruturais, a liga ferro-carbono é dividida em sete categorias com base no teor de carbono no diagrama de fases da liga ferro-carbono:
(1) Ferro puro industrial, com teor de carbono < 0,0218%;
(2) Aço eutetóide, com teor de carbono de 0,77%;
(3) Aço hipoeutetóide, com teor de carbono variando de 0,0218% a 0,77%;
(4) Aço hipereutetóide, com teor de carbono variando de 0,77% a 2,11%;
(5) Ferro fundido branco eutético, com teor de carbono de 4,30%;
(6) Ferro fundido branco subcristalino, com teor de carbono variando de 2,11% a 4,30%;
(7) Ferro fundido branco supercristalino, com teor de carbono variando de 4,30% a 6,69%.
2. Estrutura metálica
Metal: Material com boa condutividade térmica e elétrica, caracterizado por sua aparência opaca e brilho metálico. A condutividade dos metais diminui à medida que a temperatura aumenta, e eles são conhecidos pela sua ductilidade e capacidade de expansão.
Um cristal metálico é um sólido no qual os átomos estão dispostos em um padrão regular.
Liga: Substância com propriedades metálicas composta por dois ou mais elementos, incluindo metais e não metais.
Fortalecimento da solução sólida: Isso ocorre quando os átomos do soluto ocupam os espaços ou interstícios da rede do solvente, fazendo com que a rede fique distorcida e aumentando a dureza e a resistência da solução sólida.
Composto: Uma nova estrutura sólida cristalina com propriedades metálicas é formada pela combinação de componentes de liga.
Mistura Mecânica: Composição de liga composta por duas estruturas cristalinas distintas, embora apareça como uma entidade única com propriedades mecânicas independentes.
Ferrita: Uma solução sólida intersticial de carbono em alfa-Fe (ferro cúbico de corpo centrado).
Austenita: Uma solução sólida intersticial de carbono em gama-Fe (ferro cúbico de face centrada).
Cementita: Composto estável (Fe3C) formado pela combinação de carbono e ferro.
Perlita: Mistura mecânica composta por ferrita e cementita (F + Fe3C, contendo 0,8% de carbono).
Ledeburita: Mistura mecânica composta de cementita e austenita (contendo 4,3% de carbono).
O tratamento térmico de metais é um processo crucial na fabricação mecânica. Ao contrário de outros métodos de processamento, o tratamento térmico não altera a forma ou a composição química global da peça, mas em vez disso melhora o seu desempenho, modificando a sua microestrutura ou composição química da superfície.
O objetivo do tratamento térmico é melhorar a qualidade interna da peça, que muitas vezes não é visível a olho nu. Para alcançar as propriedades mecânicas, físicas e químicas desejadas de uma peça metálica, muitas vezes é necessário tratamento térmico, além da seleção apropriada de materiais e vários processos de conformação.
O aço é o material mais utilizado na indústria mecânica e sua microestrutura pode ser controlada por meio de tratamento térmico. Como resultado, o tratamento térmico do aço é um aspecto importante do tratamento térmico do metal.
Além do aço, o tratamento térmico também pode ser utilizado para modificar as propriedades mecânicas, físicas e químicas do alumínio, cobre, magnésio, titânio e suas ligas, permitindo a obtenção de diversas propriedades de serviço.